準静的過程とは、系に膨張・圧縮・加熱・冷却といった変化がゆっくり行われることで、常に平衡状態を保ちながら変化するような過程のことである。準静的過程によって変化した系は、その過程を逆向きにたどれば、再び元の状態に戻れるという特徴をもつ。
目次
準静的過程の例
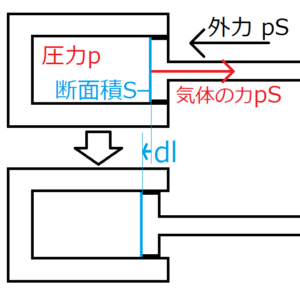
図のように、圧力\(p\)の気体を閉じ込めた断面積\(S\)のピストンを考える。
外力の強さとそれによる仕事
今、ピストン内部からの力\(pS\)と外力が釣り合っている。
この状態から外力を静かに加えていくと、外力がわずかに\(pS\)を上回るため、ピストンは内側に動く。ピストンが動いたとき、熱平衡の状態は一時的に崩れる。ところが、外力と\(pS\)の差は小さいため、熱平衡の崩れが小さいと考えられる。外力と内部からの力の差が0になる極限をとるということは、すなわち熱平衡の崩れが十分小さいという極限をとるということであり、準静的過程を満たす。以上からこの過程を、外力が\(pS\)の準静的過程として考える。
このときピストンが動いた距離を\(dl\)とおく(ピストンの進行方向を正とおいた)。すると、この過程で外力がした仕事\(W\)は、次のようになる。
\begin{eqnarray} W&=&(力)×(距離)\\&=&pS×dl \end{eqnarray}
また、図中の\(dl\)の向きは、ピストン内の体積\(V\)を減らす方向に向いている。したがって、\(dl\)と\(dV\)の符号は逆向きになる。よって、\(dV=-Sdl\)。このことを踏まえると、\(W\)は次のように変形できる。
$$W=-pdV$$
この式が、外力がした仕事\(W\)と系の体積変化\(dV\)の関係式である。
外力がした仕事\(W\)と気体がした仕事\(W’\)の関係
内部の気体がピストンを押す力と、外力は釣り合っている。これにより、気体の力と外力は互いに逆向きかつ大きさが等しい。したがって、この過程で気体がした仕事\(W’\)と外力の仕事\(W\)は、大きさは等しいが符号は逆になる。
$$W=-W’$$
以上のように、準静的過程においては、系が外にする仕事と系が受ける仕事は、大きさは等しいが符号が逆になる。
熱力学第一法則への導入
系が準静的に微小変化したときの内部エネルギーの変化は、\(d’W=-pdV\)を代入することで、次のように表せる。
$$dU=d’Q-pdV$$
準静的過程でない過程の例
上の例と同様のピストン装置をつくる。ここで、ピストンを急激に押し込むと、外力が気体の力\(pS\)を大きく上回ってしまう。これでは、熱平衡のずれが無視できなくなるため、この運動は準静的過程でない。
次に、寒い部屋の一部を急激に温めた場合を考えよう。この場合、温めた部分の温度だけが上昇していくため、部屋全体でみると平衡状態でなくなる。
まとめ
・準静的過程とは、常に系の平衡状態が保たれながら変化する過程のことである。
・ピストンによる準静的過程で外力がする仕事は、\(W=-pdV\)である。
参考文献
・三宅哲(1994)『熱力学』,裳華房.